L'acido borico, un composto chimico di notevole interesse storico e applicativo, presenta una solubilità in alcol che merita un'analisi dettagliata. Questo ossiacido del boro trivalente, scoperto nel 1702 da Hombert, è stato a lungo impiegato in svariati campi, dalla medicina all'industria, grazie alle sue proprietà antisettiche, insetticide e ignifughe. La sua interazione con solventi come gli alcoli è un aspetto fondamentale per comprenderne appieno le potenzialità e le limitazioni.
Proprietà Strutturali e Chimiche dell'Acido Borico
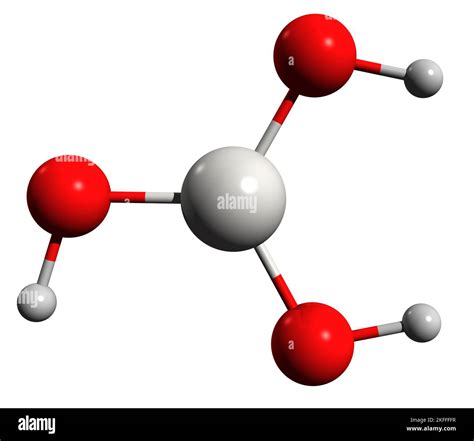
L'acido borico, noto anche con il nome IUPAC di acido triidrossiboro e con la formula chimica B(OH)₃, si presenta allo stato isolato come una molecola planare con l'atomo di boro ibridato sp². La sua struttura cristallina è caratterizzata da strati di molecole tenute insieme da legami idrogeno, una disposizione che conferisce al composto una facile sfaldatura in scaglie. Questa proprietà stratificata, con gruppi BO₃ coplanari, è alla base di alcune delle sue applicazioni, come quelle in cui sono richieste qualità lubrificanti.
Chimicamente, l'acido borico è classificato come un acido debole di Lewis, con un pKa di 5,81×10⁻¹⁰ in acqua a 25 °C (il valore di pKa è 9,24, ma la dissociazione avviene in modo non convenzionale). Nelle soluzioni acquose, si comporta come un acido debole monobasico, dissociandosi parzialmente in protoni (H⁺) e ioni borato (B(OH)₄⁻). Tuttavia, in determinate reazioni, manifesta caratteristiche che suggeriscono una natura tribasica. La sua debole acidità pone sfide per la titolazione accurata, ma l'aggiunta di agenti complessanti come il mannitolo o il sorbitolo ne aumenta significativamente l'acidità, permettendo una misurazione precisa.
L'acido borico è incompatibile con carbonati e idrossidi alcalini. Forma sali solubili con cationi monovalenti, come il borace (Na₂B₄O₇·10H₂O, solubile al 6% in acqua), e sali insolubili con cationi bivalenti.
La Solubilità in Alcol: Un Fattore Chiave
La solubilità dell'acido borico varia notevolmente a seconda del solvente. Mentre in acqua la sua solubilità aumenta con la temperatura, raggiungendo circa 27,53 g/100 mL a 100 °C, la sua interazione con gli alcoli è particolarmente interessante. Le informazioni disponibili indicano che negli alcoli la solubilità aumenta, soprattutto nel glicerolo, con solubilità che possono arrivare fino a 50 g/100 ml. Questa maggiore solubilità in alcoli rispetto all'acqua è attribuibile alla natura polare sia dell'acido borico che degli alcoli, che facilitano la formazione di legami intermolecolari.
L'alcool etilico denaturato, in particolare, viene utilizzato in combinazione con l'acido borico in diverse applicazioni industriali e mediche. Ad esempio, nell'industria orafa, la miscela di acido borico e alcool etilico denaturato serve a ridurre l'ossidazione superficiale e la comparsa di macchie sui metalli durante i processi termici come la saldatura e la ricottura.
Produzione Industriale dell'Acido Borico
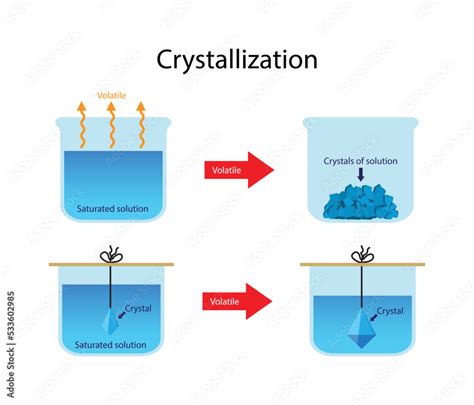
L'acido borico viene prodotto industrialmente a partire da minerali borati e salamoie. Tra i minerali più comuni utilizzati vi sono il borace, la kernite, la colemanite, l'ascharite, l'ulexite e l'idroboracite. Questi minerali reagiscono con acidi minerali forti, come l'acido solforico, per formare acido borico. Il processo industriale prevede tipicamente la separazione del materiale inerte insolubile e la cristallizzazione del prodotto desiderato. Negli Stati Uniti, i minerali di borato di sodio sono la fonte principale, mentre la Turchia impiega ampiamente la colemanite. La datolite, un minerale borosilicato, è un'altra materia prima utilizzata in alcune regioni.
Per quanto riguarda la sua presenza in natura, l'acido borico si trova come minerale sassolite.
Applicazioni Multiformi dell'Acido Borico
Le applicazioni dell'acido borico sono estremamente variegate e spaziano in numerosi settori:
- Industria: Viene impiegato nella produzione di fibre di vetro sintetiche (vetro borosilicato), smalti, adesivi (in particolare per carta e cartone, dove agisce come agente di reticolazione), fluidi industriali (antigelo, liquidi per freni, oli lubrificanti, fluidi per lavorazione dei metalli), fluidi reologici per il recupero di petrolio e gas, e come inibitore di corrosione nei sistemi di trattamento delle acque.
- Agricoltura: È un nutriente essenziale per le piante, utilizzato come fertilizzante per migliorare la qualità e le rese di colture come palma da olio, arachidi, mele, uva e barbabietole da zucchero.
- Controllo dei Parassiti: Agisce come insetticida efficace contro termiti, scarafaggi, formiche carpentiere e coleotteri distruttori del legno.
- Pulizia e Cura della Persona: Trova impiego nei prodotti per la pulizia e il bucato, contribuendo a tamponare, sospendere particelle di sporco e addolcire l'acqua.
- Materiali Ignifughi: È un efficace ritardante di fiamma per materiali cellulosici come legno e ovatta di cotone, e viene aggiunto ai polimeri per migliorarne la resistenza al fuoco.
- Metallurgia: Utilizzato in operazioni di fusione, trafilatura, borurazione, brasatura, saldatura e produzione di leghe.
- Industria Nucleare: Impiegato nei reattori ad acqua pressurizzata come "veleno" per neutroni, per controllare la reazione nucleare. È stato utilizzato anche in seguito all'incidente di Chernobyl per prevenire ulteriori reazioni.
- Piromecnica: Aggiunto in piccole percentuali per prevenire la formazione di ammidi e come colorante per la fiamma (verde).
- Lubrificanti: Sospensioni colloidali di nanoparticelle di acido borico in oli possono formare eccellenti lubrificanti.
ACIDO BORICO PARA QUE SIRVE | 3 COSAS
Utilizzo in Ambito Medico e Otorinolaringoiatrico
In medicina, l'acido borico è noto per le sue proprietà antisettiche, antibatteriche e antimicotiche. Viene utilizzato:
- Come antisettico: per piccole ustioni o ferite, e in soluzioni molto diluite per l'irrigazione oftalmica.
- Per la cura delle infezioni cutanee: inclusa l'acne e la prevenzione delle micosi.
- In ambito otorinolaringoiatrico: soluzioni acquose o alcoliche di acido borico (spesso al 3%) sono impiegate per la pulizia delle orecchie e per il trattamento o la prevenzione delle infezioni dell'orecchio esterno (otite esterna, otomicosi). L'alcool al 70% in combinazione con acido borico può essere utilizzato per trattare alcuni tipi di infezioni dell'orecchio.
È importante notare che l'uso dell'acido borico in queste applicazioni deve avvenire sotto supervisione medica, prestando attenzione alla concentrazione e al metodo di applicazione, soprattutto in presenza di traumi o lesioni cutanee, perforazioni del timpano o in età pediatrica. L'orecchio è un organo delicato e un uso improprio può portare a secchezza, prurito, infiammazione e, in casi estremi, danni all'udito.

Tossicologia e Precauzioni
L'acido borico presenta una bassa tossicità acuta. Non è considerato cancerogeno o mutageno, né un irritante o sensibilizzante cutaneo. Tuttavia, può causare effetti sullo sviluppo in animali da laboratorio e potenziali effetti avversi sulla riproduzione maschile negli animali, sebbene l'evidenza di effetti negli esseri umani sia limitata.
I limiti di esposizione occupazionale sono di 2 mg/m³. L'ingestione di quantità significative (5 g o più) può irritare il tratto gastrointestinale e influenzare il sistema nervoso centrale. Il contatto con la polvere o soluzioni acquose può irritare gli occhi. È consigliabile evitare un'esposizione prolungata.
Le normative europee (Regolamento (UE) n. 231/2012) e le schede di sicurezza degli agenti chimici forniscono indicazioni dettagliate sui pericoli associati all'acido borico, tra cui la potenziale compromissione della fertilità e danni al feto (frase H360FD). Pertanto, è fondamentale ottenere istruzioni specifiche prima dell'uso e utilizzare dispositivi di protezione individuale appropriati.
Conclusioni Parziali sulla Solubilità
In sintesi, la solubilità dell'acido borico in alcol, in particolare in etanolo e glicerolo, è significativamente maggiore rispetto alla sua solubilità in acqua. Questa proprietà è sfruttata in diverse applicazioni dove è necessario un solvente organico per la sua azione discioglitrice, come nella preparazione di soluzioni antisettiche per uso auricolare o in formulazioni industriali specifiche. La comprensione di questa differenza di solubilità è cruciale per la formulazione corretta di prodotti a base di acido borico e per ottimizzarne l'efficacia in base all'applicazione desiderata.
L'acido borico è un composto chimico versatile, la cui interazione con gli alcoli apre la porta a una gamma di utilizzi che vanno ben oltre le sue ben note proprietà mediche e domestiche, estendendosi a processi industriali complessi e a tecnologie avanzate.
tags: #acido #borico #solubilita #alcol