La Graft-versus-Host Disease (GVHD), o Malattia del Trapianto contro l'Ospite, rappresenta una delle complicanze immunologiche più significative e temute nel contesto del trapianto di cellule staminali emopoietiche allogeniche (HSCT). Questa patologia, di natura immunologica, si manifesta quando le cellule immunitarie del donatore, appena trapiantate, riconoscono i tessuti del ricevente come estranei e avviano una risposta immunitaria aggressiva contro di essi. La GVHD è considerata la principale causa di insuccesso nel trapianto allogenico di cellule staminali emopoietiche e costituisce una delle complicanze più comuni, con un'incidenza stimata tra il 40-60% dei casi e una mortalità associata che si attesta intorno al 15% nei casi non recidivanti post-HSCT.
Meccanismi Patogenetici: Un Attacco Immunitario Sbilanciato
Il processo patogenetico della GVHD è mediato principalmente dai linfociti T del donatore. Dopo il regime preparatorio per il trapianto, che mira a eliminare le cellule maligne del ricevente ma compromette anche il suo sistema immunitario, le cellule T del donatore diventano attive. Queste cellule, dotate di immunocompetenza, riconoscono gli antigeni del donatore (in particolare quelli del complesso maggiore di istocompatibilità, HLA) presenti sulle cellule del ricevente come "non-self". Questo riconoscimento innesca una cascata infiammatoria caratterizzata da un'elevata produzione di citochine pro-infiammatorie, come il TNF-alfa e l'IFN-gamma. Questa attivazione "sbilanciata" del sistema immunitario porta a un danno tissutale esteso, colpendo prevalentemente organi come la cute, il fegato e il tratto gastrointestinale. I criteri fondamentali perché si determini la GVHD, noti come criteri di Billingham, includono: l'incapacità dell'ospite di rigettare il trapianto, la presenza di cellule immunocompetenti nel trapianto, e la diversità genetica tra donatore e ricevente.
Manifestazioni Cliniche: Dalla Forma Acuta alla Cronica
La GVHD si manifesta clinicamente in due forme principali: acuta e cronica, distinte in base al tempo di insorgenza e alle caratteristiche cliniche.
La Forma Acuta (aGvHD)
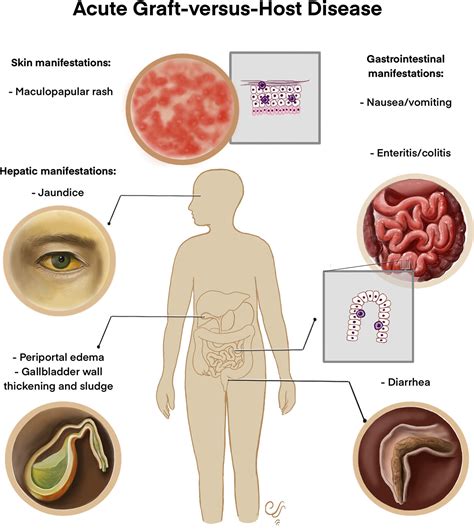
La forma acuta della malattia si osserva tipicamente nei primi 100 giorni dalla data del trapianto. È caratterizzata da un danno acuto alle cellule epiteliali di diversi organi. Le manifestazioni più comuni coinvolgono tre organi principali:
- Cute: Si presenta con eruzioni cutanee, che vanno da un eritema maculo-papulare a forme più diffuse come l'eritrodermia o la desquamazione. L'eruzione inizia spesso sui palmi delle mani, sulle piante dei piedi, sul collo o sulle orecchie, per poi diffondersi. La cute può diventare secca, pruriginosa e tesa, talvolta con fibrosi. Possono verificarsi anche perdita di capelli e alterazioni delle unghie.
- Apparato Gastrointestinale: I sintomi includono nausea, vomito, dolori addominali crampiformi e una grave diarrea acquosa. La gravità del coinvolgimento gastrointestinale è valutata in base alla quantità di feci diarroiche giornaliere o al numero di evacuazioni.
- Fegato: Si manifesta con epatite e ittero, valutati sulla base dei livelli di bilirubina.
La diagnosi della GVHD acuta è primariamente clinica, ma può essere supportata da biopsie tissutali mirate. Queste biopsie sono essenziali per differenziare la GVHD da altre condizioni confondenti, come infezioni virali (epatite, colite) o reazioni avverse a farmaci. La gravità della GVHD acuta è classificata in gradi da 0 a 4, secondo la stadiazione classica di Glucksberg, basata sul coinvolgimento organo-specifico e sulla severità globale. I pazienti affetti da GVHD di grado 3 o 4 hanno una prognosi infausta.
La Forma Cronica (cGVHD)
La forma cronica della GVHD, invece, decorre dopo i primi 100 giorni dal trapianto e può persistere per anni. È caratterizzata da fibrosi e atrofia degli organi colpiti anche dalla forma acuta, ma senza un'evidente morte cellulare acuta. Oltre ai classici organi bersaglio (cute, fegato, tratto gastrointestinale), la GVHD cronica può coinvolgere i polmoni, causando obliterazione delle vie aeree e potenzialmente portando a insufficienza respiratoria.
Le manifestazioni della cGVHD possono includere:
- Cute e Annessi: Fibrosi cutanea, secchezza, prurito, perdita di capelli e alterazioni delle unghie.
- Bocca: La GVHD orale cronica è una complicanza frequente, che può interessare la popolazione di pazienti in età più avanzata. Si manifesta con secchezza delle fauci (xerostomia), alterazioni del gusto (diseugesia), deficit deglutitori e masticatori. Possono svilupparsi mucoceli superficiali all'interno delle labbra e del palato, con un aumentato rischio di lesioni cariose, specialmente lungo la linea gengivale e interprossimalmente.
- Ghiandole Salivari: La cGVHD orale può compromettere la funzionalità delle ghiandole salivari.
- Polmoni: Può causare fibrosi polmonare e obliterazione delle vie aeree, con conseguente insufficienza respiratoria.
La GVHD cronica, sebbene raramente fatale nell'immediato, può causare disabilità permanenti che impattano severamente sulla qualità della vita del paziente.
Terapia della malattia del trapianto contro l'ospite (GVHD)
Fattori di Rischio e Prevenzione
La frequenza e la gravità della GVHD aumentano in base al grado di diversità genetica tra donatore e ricevente, in particolare per quanto riguarda il sistema HLA (Human Leukocyte Antigen). Una minore compatibilità HLA è il fattore di rischio più significativo. Altri fattori di rischio per la GVHD acuta includono l'età avanzata del ricevente, un donatore parzialmente compatibile o alloimmunizzato, e un'immunosoppressione meno intensa.
La profilassi rappresenta la strategia più efficace per la gestione della GVHD. Tradizionalmente, la prevenzione si è basata sull'utilizzo di una combinazione di inibitori della calcineurina, come la ciclosporina A (CSA) o il tacrolimus (FK506), associati al metotrexato (MTX). Sebbene questi regimi abbiano ridotto l'incidenza di GVHD acuta, l'intensificazione dell'immunosoppressione ha spesso comportato un aumento del rischio di infezioni gravi o recidive di malattia, senza peraltro migliorare significativamente la GVHD cronica.
Negli ultimi anni, sono stati sviluppati approcci più sofisticati per la profilassi. Uno studio di fase 3 (BMT CTN 1703) ha confrontato una combinazione a tre farmaci composta da ciclofosfamide post-trapianto, tacrolimus e micofenolato mofetile (PTCy/Tac/MMF) con il regime standard Tac/MTX in pazienti sottoposti a trapianto allogenico di cellule staminali emopoietiche con regime di condizionamento a ridotta intensità (RIC). I risultati hanno dimostrato che il regime PTCy/Tac/MMF riduce significativamente il rischio di GRFS (Graft-versus-Host Disease-Free, Relapse-Free Survival), un endpoint composito che include l'insorgenza di GVHD acuta di grado III-IV, GVHD cronica richiedente terapia immunosoppressiva sistemica, recidiva o progressione di malattia, e morte per qualsiasi causa. Il tasso di GRFS a 1 anno è risultato significativamente più elevato nel gruppo trattato con PTCy/Tac/MMF (52,7%) rispetto al gruppo di controllo (34,9%). Inoltre, i tassi di GVHD acuta di grado III-IV al giorno 100 erano inferiori (6,3% vs 14,7%) e i tassi di GVHD cronica a 1 anno erano anch'essi ridotti (21,9% vs 35,1%) nel braccio PTCy/Tac/MMF. Questi risultati suggeriscono che la combinazione PTCy/Tac/MMF potrebbe diventare uno standard di trattamento per la prevenzione della GVHD, anche in trapianti da donatori altamente correlati con regimi di condizionamento a intensità ridotta.
La profilassi con globulina antilinfocitaria (ATG) o la deplezione selettiva delle cellule T ex vivo sono altre strategie utilizzate per ridurre l'incidenza di GVHD.
Gestione Terapeutica della GVHD
La gestione della GVHD acuta, specialmente nei gradi avanzati (III-IV), richiede un approccio aggressivo e multispecialistico.
Terapia di Prima Linea
Il pilastro della terapia per la GVHD acuta è stato a lungo rappresentato dai corticosteroidi ad alte dosi, in particolare il metilprednisolone (generalmente alla dose di 2 mg/kg/die). Ci si può aspettare che questi farmaci raggiungano risposte nel 40-60% dei pazienti. Tuttavia, dosi più elevate di steroidi non hanno dimostrato benefici aggiuntivi.
Terapia di Seconda Linea e Farmaci Innovativi
Per i pazienti che non rispondono alla terapia steroidea iniziale (GVHD steroide-refrattaria), le opzioni terapeutiche di seconda linea sono meno definite e associate a una prognosi peggiore. L'associazione con altri farmaci immunosoppressori, come la ciclosporina, il tacrolimus, il micofenolato mofetile, o farmaci biologici come gli inibitori del TNF-alfa, è stata esplorata con risultati variabili.
Un recente sviluppo promettente è l'uso di Ruxolitinib, un inibitore della Janus chinasi 1/2 (JAK1/2). Questo farmaco ha dimostrato efficacia nel trattamento della GVHD acuta steroide-refrattaria ed è stato recentemente approvato dalla FDA americana per questa indicazione. Studi recenti hanno anche evidenziato una migliore risposta, sebbene non una riduzione della mortalità, con steroidi associati a Ruxolitinib.
Un'altra area di ricerca emergente riguarda l'utilizzo delle cellule staminali mesenchimali (MSC). Le MSC possiedono importanti proprietà immunomodulatorie, essendo in grado di diminuire la produzione di citochine pro-infiammatorie e aumentare quelle anti-infiammatorie. Questo le rende potenzialmente capaci di arrestare il processo patologico alla base della GVHD e favorire la rigenerazione tissutale. Studi preliminari hanno riportato risultati incoraggianti nel trattamento di pazienti con aGvHD di grado III-IV refrattaria alla terapia steroidea, utilizzando MSC di derivazione adipocitaria espanse ex vivo.
Gestione delle Manifestazioni Specifiche
La gestione della GVHD richiede anche un'attenta cura delle manifestazioni specifiche e delle complicanze associate:
- GVHD Cutanea: Il trattamento può includere l'uso di emollienti, corticosteroidi topici e, nei casi più severi, la terapia sistemica. È fondamentale anche il trattamento delle infezioni cutanee secondarie.
- GVHD Gastrointestinale: Oltre alla terapia sistemica, è essenziale un'alimentazione appropriata per gestire la diarrea e prevenire la malnutrizione. Possono essere necessari supporti nutrizionali.
- GVHD Orale: Per alleviare il dolore orale associato alla GVHD e alla xerostomia, possono essere utilizzati anestetici topici come la lidocaina in gel. Farmaci atti a stimolare l'attività delle ghiandole salivari o presidi medici per alleviare la secchezza delle fauci possono essere di beneficio.
Monitoraggio e Approccio Integrato
La gestione della GVHD acuta comporta un aggressivo monitoraggio delle infezioni batteriche, fungine e virali, con terapia pre-emptiva quando indicata. La terapia di supporto, che include il supporto alimentare e trasfusionale, è altrettanto cruciale.
La GVHD rappresenta ancora oggi una sfida complessa che necessita di un approccio integrato, che coinvolga team medici multidisciplinari (ematologi, dermatologi, gastroenterologi, pneumologi, infettivologi, specialisti di cure palliative) e infermieristici. Il controllo simultaneo della GVHD e della recidiva di malattia è di fondamentale rilevanza per il successo del trapianto allogenico. Il monitoraggio post-trapianto deve essere costante per identificare precocemente l'insorgenza di GVHD e intervenire tempestivamente.
La ricerca continua a esplorare nuovi biomarcatori per una diagnosi più precoce e precisa e per una migliore stratificazione del rischio, al fine di superare le attuali classificazioni cliniche e ottimizzare ulteriormente le strategie terapeutiche.
tags: #gradazione #gvh #acuta